近日,济南大学刘宏教授、王树萍副教授联合山东大学齐鲁医院周恒星教授及中国科学院深圳先进技术研究院王泽南研究员提出了一种纳米药物介导的“细胞内小分子/离子风暴”激活神经再生促进脊髓损伤修复的新方法。相关成果以“Intracellular small molecule/ion storm from Ca-phytate nanoparticle synergizes neural stem cell therapy and immunomodulation in spinal cord injury”为题发表在生物材料领域权威期刊Biomaterials(IF=12.9)。文章第一作者为济南大学2022级硕士研究生时佳培、2024级博士研究生张朔和山东大学博士后冯彦斌,通讯作者为刘宏教授、王树萍副教授、周恒星教授和王泽南研究员,济南大学为第一完成单位。

脊髓损伤是一种毁灭性的中枢神经系统创伤,多由交通事故、高处坠落等意外事件引起。据统计,全球约有1500万至2000万人受其影响,每年新增病例近90万。该疾病不仅导致患者感觉、运动和自主神经功能严重丧失,造成极高的致残率,也为家庭和社会带来沉重的经济负担。当前,脊髓损伤的治疗面临两大核心挑战:一是受损神经元固有的再生能力极弱,二是损伤区域持续的炎症微环境严重阻碍修复进程。神经干细胞移植虽为再生带来希望,但移植后的干细胞能否成功分化为功能神经元,以及如何应对“敌意”的炎症环境,是决定疗效的关键。因此,理想的治疗策略需要“双管齐下”:既能引导干细胞定向分化为神经元,又能将有害的促炎微环境逆转为有益的修复型微环境。
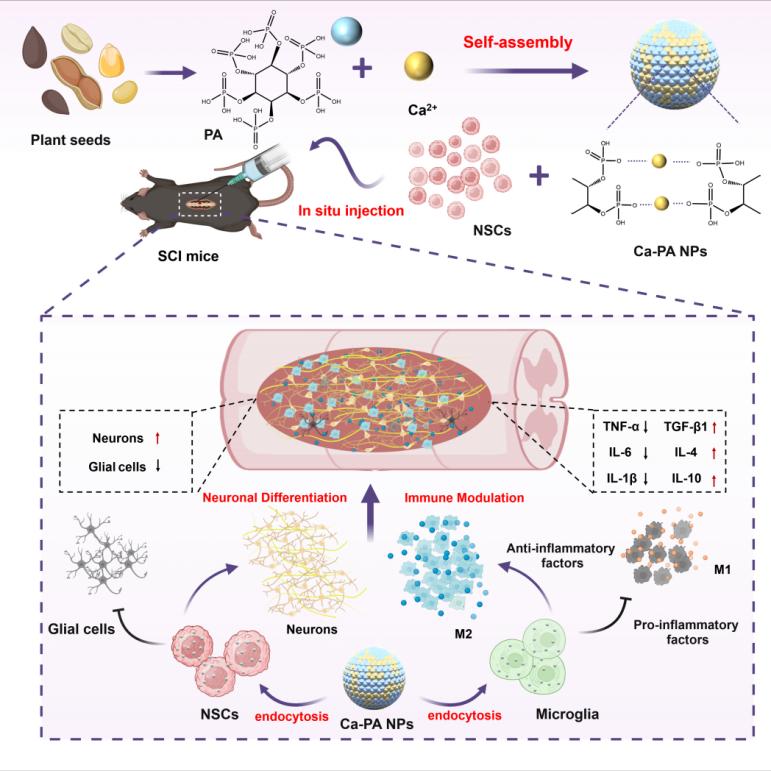
针对上述问题,研究团队从天然产物中寻找灵感,设计了一种新型的智能响应型调节剂——植酸钙纳米药物(Ca-PA NPs),其通过细胞内吞作用高效进入神经干细胞和小胶质细胞。在细胞内部的酸性溶酶体环境中,纳米颗粒迅速分解,瞬间释放出高浓度的游离植酸和钙离子,形成“细胞内小分子/离子风暴”,实现对细胞命运的精准调控。该纳米药物不仅定向诱导神经干细胞向功能神经元分化,还可逆转小胶质细胞从促炎M1表型向修复型M2表型重编程。在脊髓半横断损伤的小鼠模型中,纳米药物与神经干细胞共移植后,小鼠的后肢运动功能、感觉功能以及自主神经功能均得到显著改善。损伤区域呈现功能性神经元再生及胶质瘢痕减少,同时炎症细胞浸润被有效抑制,神经再生微环境得到重塑。这项研究成功开发出一种新型纳米调节剂,兼具精准调控干细胞命运与重塑免疫微环境的双重功能,为开发用于脊髓损伤及其他神经系统疾病的下一代组合型纳米药物提供了全新思路与实验基础。通过功能化纳米药物的靶向性与递送效率,该类创新制剂有望拓展至阿尔茨海默病、帕金森病等神经退行性疾病的治疗领域,展现出重要的临床转化潜力。
近年来,刘宏教授带领的济南大学细胞诊疗与生物传感器团队在干细胞治疗及生物检测领域取得多项原创突破性研究成果(Adv.Mater.,Adv.Funct.Mater.,ACS Nano,Biomaterials,Adv.Sci.,Adv.Healthc.Mater.,Small,BMEMat)。相关工作得到了国家重点研发计划、国家自然科学基金、国家高层次青年人才计划、山东省自然科学基金、山东省泰山学者计划、济南市科技局和济南大学的大力支持。
原文信息:
Shi J, Feng Y, Zhang S, et al. Intracellular small molecule/ion storm from Ca-phytate nanoparticle synergizes neural stem cell therapy and immunomodulation in spinal cord injury. Biomaterials. 2025. https://doi.org/10.1016/j.biomaterials.2025.123708
撰稿:王树萍 编辑:刘孟頔 编审:张伟